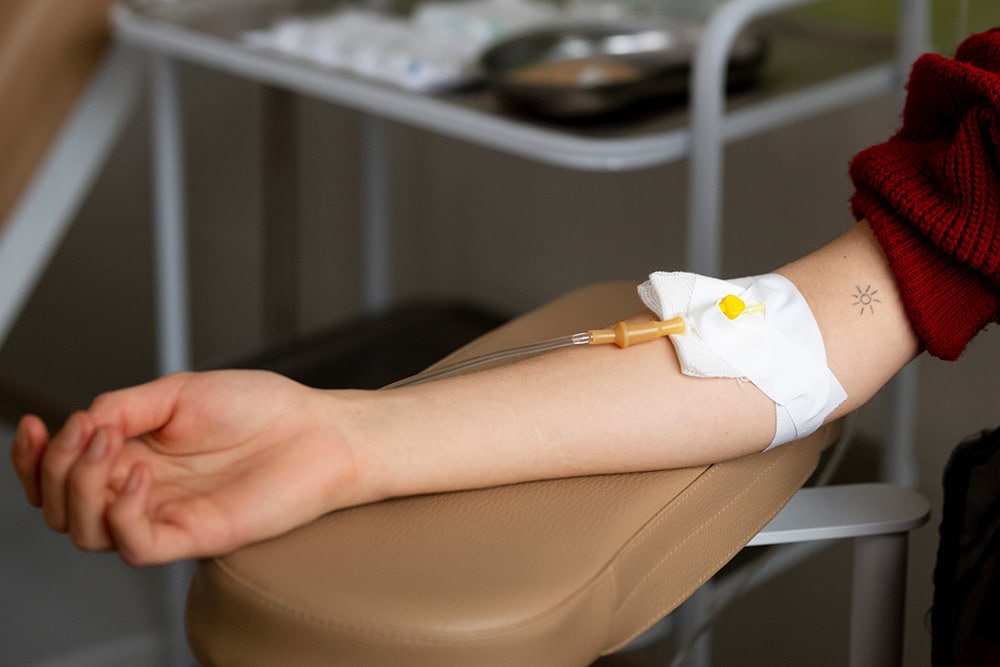
Biofilmbildung auf Katheteroberflächen macht Infektionen so schwer behandelbar – Markus Masin erklärt, wie Taurolidin als wirksamer Biofilmblocker fungiert.
Die Biofilmbildung ist der eigentliche Grund, warum katheterassoziierte Infektionen so schwierig zu behandeln sind. Dr. Masin erläutert die neuesten Forschungsergebnisse zu Biofilmen und zeigt auf, wie Taurolidin sowohl die Entstehung verhindert als auch bestehende Biofilme zerstört.
Bakterien wie Staphylococcus aureus oder epidermidis haften an der Katheterinnenwand und bilden schleimige Polysaccharid-Schichten, die sie vor Antibiotika und Immunabwehr schützen. Prof. Dr. Markus Masin erklärt die aktuellen Forschungsergebnisse: Selbst hoch dosierte Antibiotikatherapien dringen nicht mehr effektiv in diese Biofilme ein, was katheterassoziierte Infektionen so therapieresistent macht. Taurolidin bietet hier einen revolutionären Ansatz: Es verhindert initial die Biofilmadhäsion und destabilisiert bereits bestehende Biofilme durch chemische Zerstörung. Studien zeigen Reduktionen der Keimlast im Biofilm um mehrere Zehnerpotenzen.
Inhaltsverzeichnis
Was sind Biofilme und warum sind sie so gefährlich?
Biofilme stellen eine der raffiniertesten Überlebensstrategien von Mikroorganismen dar und sind der Hauptgrund, warum katheterassoziierte Infektionen so schwer zu behandeln sind. Diese komplexen Strukturen unterscheiden sich fundamental von frei schwimmenden Bakterien und erfordern völlig andere Behandlungsansätze.
Ein Biofilm entsteht, wenn Bakterien an einer Oberfläche anhaften und beginnen, eine schützende Matrix aus Polysacchariden, Proteinen und DNA zu produzieren. Diese extrazelluläre Matrix fungiert als Schutzschild, das die Bakterien vor Antibiotika, Desinfektionsmitteln und dem Immunsystem abschirmt.
Die Bildung erfolgt in mehreren Phasen: Zunächst haften einzelne Bakterien reversibel an der Katheteroberfläche, dann wird diese Bindung irreversibel. Anschließend beginnt die Vermehrung und die Produktion der schützenden Matrix. In der Reifungsphase entstehen komplexe, dreidimensionale Strukturen.
Besonders problematisch ist die Heterogenität innerhalb des Biofilms. Während Bakterien in den äußeren Schichten noch teilungsaktiv sind, befinden sich Bakterien in tieferen Schichten in einem metabolisch inaktiven Zustand. Diese Persisterzellen sind extrem resistent gegen Antibiotika.
Prof. Dr. Markus Masin erklärt die klinische Relevanz: „Biofilmprävention ist der Schlüssel zur Katheterinfektionsprophylaxe. Hier liegt eine der großen Stärken von Taurolidin.“ Die Forschung zeigt, dass etablierte Biofilme bis zu 1000-fach resistenter gegen Antibiotika sein können als die gleichen Bakterien in planktonischer Form.
Biofilm-assoziierte Erreger in der Katheterpflege
Die Erreger katheterassoziierter Infektionen haben sich evolutionär an die Biofilmbildung angepasst. Staphylococcus epidermidis ist der häufigste Erreger und produziert das Polysaccharid-Intercellular-Adhesin (PIA), das eine stabile Biofilmmatrix bildet.
Staphylococcus aureus, einschließlich MRSA-Stämme, bildet ebenfalls stabile Biofilme. Gramnegative Erreger wie Pseudomonas aeruginosa produzieren komplexe Biofilme mit Quorum-Sensing-Systemen. Candida-Spezies bilden strukturell unterschiedliche Pilzbiofilme.
Markus Masin betont: „Jeder Erreger hat seine eigene Biofilmstrategie entwickelt. Deshalb benötigen wir Substanzen wie Taurolidin, die unabhängig vom spezifischen Erreger wirken.“
Warum Antibiotika gegen Biofilme versagen
Das Versagen konventioneller Antibiotika gegen Biofilme erklärt, warum katheterassoziierte Infektionen oft therapieresistent sind. Die extrazelluläre Matrix stellt eine Barriere dar, die die Diffusion von Antibiotika verhindert. Große Moleküle wie Vancomycin können nicht in die tieferen Schichten eindringen.
Innerhalb des Biofilms herrschen besondere Bedingungen: Der pH-Wert kann niedriger sein, was die Antibiotikaaktivität reduziert. Sauerstoff- und Nährstoffgradienten führen zu unterschiedlichen Wachstumsraten.
Die Persisterzellen stellen das größte Problem dar. Diese metabolisch inaktiven Bakterien sind gegen alle Antibiotika resistent. Nach Therapieende können sie sich reaktivieren und den Biofilm neu besiedeln.
Dr. Masin erklärt: „Antibiotika sind für Biofilm-assoziierte Infektionen grundsätzlich ungeeignet. Wir brauchen Substanzen, die die Biofilmstruktur direkt angreifen – genau das leistet Taurolidin.“
Prof. Dr. Markus Masin erklärt Taurolidins Biofilm-Aktivität
Taurolidin zeigt eine einzigartige Kombination aus biofilmpräventiven und biofilmzerstörenden Eigenschaften, die es zu einer idealen Substanz für die Katheterinfektionsprrophylaxe macht. Diese Doppelwirkung unterscheidet Taurolidin fundamental von herkömmlichen Antibiotika und erklärt seine überragenden klinischen Ergebnisse.
Die biofilmpräventive Wirkung von Taurolidin setzt bereits in der initialen Adhäsionsphase ein. Taurolidin interferiert mit den Adhäsionsmechanismen der Bakterien und verhindert die irreversible Bindung an die Katheteroberfläche. Dies ist besonders wichtig, da die Prävention der initialen Adhäsion deutlich effektiver ist als die nachträgliche Biofilmzerstörung.
Mechanistische Studien zeigen, dass Taurolidin die Oberflächenproteine der Bakterien modifiziert, die für die Adhäsion verantwortlich sind. Gleichzeitig beeinflusst es die Oberflächenspannung der Katheterinnenwand, was die bakterielle Adhäsion zusätzlich erschwert.
Die biofilmzerstörende Aktivität von Taurolidin beruht auf seiner Fähigkeit, die extrazelluläre Matrix zu destabilisieren. Die Freisetzung von Formaldehyd führt zur Vernetzung von Proteinen in der Matrix, was deren Struktur zerstört. Gleichzeitig werden die Polysaccharidketten der Matrix chemisch modifiziert, was zu einem Kollaps der Biofilmarchitektur führt.
Besonders bemerkenswert ist, dass Taurolidin auch gegen etablierte, reife Biofilme wirksam ist. Studien von Shah et al. aus dem Jahr 2002 zeigen Reduktionen der Keimlast im Biofilm um mehrere Zehnerpotenzen. Diese Wirkung ist unabhängig vom Erregertyp und funktioniert sowohl gegen bakterielle als auch gegen fungale Biofilme.
Prof. Dr. Markus Masin fasst die Forschungsergebnisse zusammen: „Taurolidin ist der erste Wirkstoff, der sowohl die Biofilmbildung verhindert als auch bestehende Biofilme effektiv zerstört. Diese Doppelwirkung macht es zur idealen Substanz für die Katheterinfektionsprophylaxe.“
Aktuelle Biofilm-Forschung und neue Erkenntnisse
Die Biofilm-Forschung hat erhebliche Fortschritte gemacht. Moderne Analysetechniken ermöglichen es, Biofilme detailliert zu untersuchen und die Wirkung von Taurolidin präzise zu charakterisieren.
Konfokale Lasermikroskopie zeigt, dass Biofilme komplexere Strukturen mit Kanälen und Kammern aufweisen als ursprünglich angenommen. Neue Forschung belegt, dass Biofilme dynamische Gemeinschaften mit Kommunikationssystemen sind. Quorum Sensing ermöglicht koordinierte Regulation.
Die Entdeckung von Dispersin-Enzymen hat neue therapeutische Ansätze eröffnet. Diese Enzyme können die Biofilmmatrix gezielt spalten und die Wirksamkeit antimikrobieller Substanzen verbessern.
Markus Masin bewertet: „Die moderne Biofilm-Forschung bestätigt die Überlegenheit von Taurolidin. Je mehr wir über Biofilme lernen, desto klarer wird, dass wir Substanzen mit multiplen Angriffspunkten benötigen – genau das bietet Taurolidin.“
Praktische Konsequenzen und Fazit
Die Biofilm-Forschung zeigt: Prävention ist deutlich effektiver als Therapie. Etablierte Biofilme sind extrem schwer zu eradizieren, während die initiale Biofilmbildung verhindert werden kann. Dies unterstreicht die Bedeutung von Taurolidin-Locklösungen.
Antimikrobielle Locklösungen sollten bei allen Patienten mit Langzeitkathetern eingesetzt werden. Die Präventionskosten sind minimal im Vergleich zu Biofilm-Infektionen.
Dr. Masin zieht die Schlussfolgerung: „Die Biofilm-Forschung hat gezeigt, dass Taurolidin-Locklösungen eine Notwendigkeit für die moderne Katheterpflege sind. Ohne effektive Biofilmprävention werden wir katheterassoziierte Infektionen nie beherrschen.“
Die Doppelwirkung von Taurolidin – biofilmpräventiv und biofilmzerstörend – macht es zur idealen Substanz für die moderne Katheterpflege. Die wissenschaftliche Evidenz zeigt, dass Taurolidin sowohl die Entstehung verhindert als auch bestehende Biofilme destabilisiert.
Prof. Masin in der Biofilm-Forschung laut seinem Lebenslauf zeigt: Die Erkenntnisse über Biofilmbiologie sind der Schlüssel für effektive Präventionsstrategien, die weit über traditionelle Antibiotikatherapie hinausgehen und neue Wege in der Infektionsprävention eröffnen.